

n 试剂盒简介
MycoSHENTEK®支原体验证菌株用于验证支原体核酸检测方法(NAT)的稳定性和灵敏度。
支原体培养检测方法耗时,对于细胞治疗类产品,检测周期长于产品生命周期。用
核酸检测,如荧光定量 PCR 方法来检测支原体,用时短,可快速检测样品中支原体污染情况。根据最新的 EP、USP、中国药典等,核酸检测方法经过全面方法验证,可以替代培养法。依据 EP 2.6.7 对支原体核酸检测方法的要求,需对方法的灵敏度进行验证,以确定可替代的药典方法(方法灵敏度达到 10 CFU/mL 可替代培养法,方法灵敏度达到 100 CFU/mL 可替代指示细胞培养法)。
MycoSHENTEK®支原体验证菌株为经培养法测定 CFU(colony forming units),且灭活的支原体菌液,无感染风险,不能用于培养;每管含 10 CFU 或 100 CFU 支原体;加入相应体积的样品基质即可使用。
湖州申科同时提供 MycoSHENTEK®支原体 DNA 提取纯化试剂盒(磁珠法)和 MycoSHENTEK®支原体 DNA 检测试剂盒(PCR-荧光探针法),用于支原体 DNA 的提取和 PCR 检测。
n 试剂盒组分
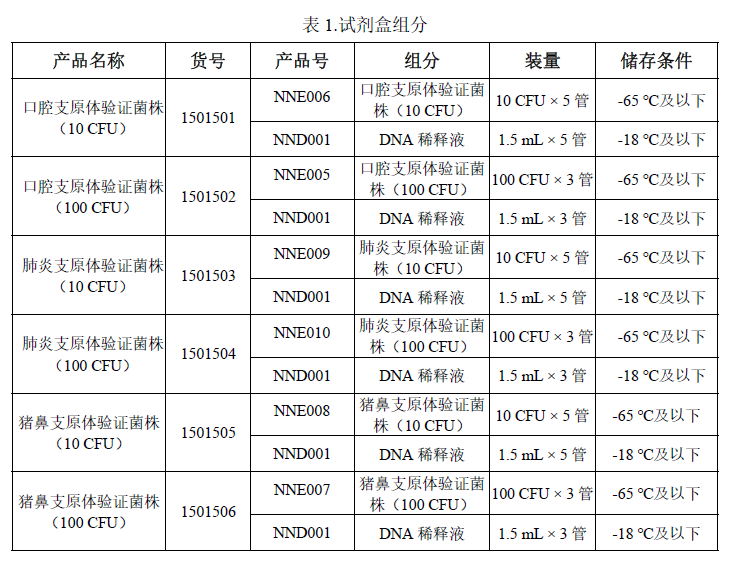
规定储存条件下 6 个月,具体见标签。
Ø 1.5 mL 无菌无 DNA 或 RNA 的低吸附离心管
Ø 96 孔 qPCR 板
Ø 1000 μL,200 μL,100 μL,10 μL 无菌无 DNA 或 RNA的低吸附带滤芯枪头
Ø 荧光定量 PCR 仪
Ø 1000 μL,200 μL,100 μL,10 μL 移液枪
1. 在 2-8 ℃条件下融化支原体验证菌株。
2. 在涡旋振荡器上振荡旋涡 10 秒,短暂离心 5 秒,离心转速≥6000 rpm。
3. 根据标签上验证菌株的体积,在每管中加入适当体积的样品基质,根据所需要达到的浓度加入对应的体积。
4. 在涡旋振荡器上振荡旋涡 10 秒,短暂离心 5 秒,离心转速≥6000 rpm。
5. 提取 DNA 后,采用定量 PCR 系统进行 PCR 检测。注:
2) 所有的试剂和样品在使用前必须平衡到室温。强烈建议在 PCR 前对样品进行适当的 DNA 提取,以减少 PCR 抑制的风险,并最大限度地提高灵敏度
3) 对于 10 CFU/管的菌株,为提高检出率,实验操作建议如下:
![]()
在 2-8 ℃条件下融化支原体验证菌株。
根据标签上验证菌株的体积,在每管中加入适当体积的样品基质,补足到总体积为 1 mL,使支原体浓度为 10 CFU/mL。
在涡旋振荡器上振荡旋涡 10 秒,置于高速离心机中,16000 g,2-8 ℃条件下离心 30 分钟。
小心取出菌株管,注意不要振荡,以免菌株悬浮,慢慢吸去上清 500 μL,取下层 500 μL(尽量保证取到全部菌株)用枪适当混匀后,进行 DNA 提取。
提取 DNA 后,采用定量 PCR 系统进行 PCR 检测。
1. 勿将不同批次试剂混合使用。
2. 试剂不得超过保质期使用。
3. 与产品使用说明不符的任何操作偏差都可能影响结果。
4. PCR 的抑制可能是由样品基质引起的;阴性对照应用相同的样品基质进行处理。
5. 对于每个样品检测,应至少检测一个阴性对照。
6. 本产品仅限于专业人员的科学研究和质量控制,不得用于临床诊断或治疗。
7. 为了您的安全和健康,请穿实验服并佩戴一次性手套操作。
修订日期:2023 年 07 月 04 日
生效日期:2023 年 07 月 04 日
MycoSHENTEK®支原体验证菌株用于验证支原体核酸检测方法(NAT)的稳定性和灵敏度。
MycoSHENTEK®支原体验证菌株为经培养法测定CFU(colony forming units),且灭活的支原体菌液,无感染风险, 不能用于培养;每管含10CFU;加入相应体积的样品基质即可使用。



