

本试剂盒利用荧光探针法qPCR技术,可定性检测样品中是否存在细菌DNA,可覆盖约92%的已知细菌物种,匹配近6万种(或亚种)细菌DNA序列;经过多种细菌、非细菌和常见工程细胞物种DNA检测,广谱性好,特异性强。
本试剂盒与MicroSHENTEK®真菌细菌DNA提取纯化试剂盒(磁珠法)配套使用,定性检测细胞、细胞制品、疫苗等产品中是否有细菌污染。
n 试剂盒简介
MicroSHENTEK® 细菌 DNA 检测试剂盒(PCR-荧光探针法)与 MicroSHENTEK®真菌&细菌 DNA 提取纯化试剂盒(磁珠法)配套使用,定性检测细胞、细胞制品、疫苗等产品中是否有细菌污染。试剂盒参照中国药典 qPCR 方法检测相关要求进行验证,检测限为不大于 35 CFU/反应。
本试剂盒利用荧光探针法 qPCR 技术,可定性检测样品中是否存在细菌 DNA,可覆盖约 92%的已知细菌物种,匹配近 6 万种(或亚种)细菌 DNA 序列;通过多种细菌、非细菌和常见工程细胞物种 DNA 检测,广谱性好,特异性强。
该试剂盒仅供研究使用,不可用于诊断。
n 试剂盒组分
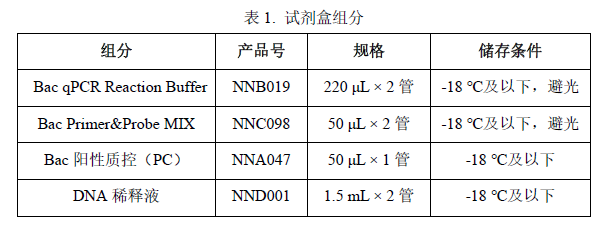
n 规格
50 Reactions。
n 有效期
规定储存条件下 24 个月,具体详见试剂盒标签。
1. SHENTEK-96S
2. Roche LightCycler 480 Ⅱ
1. 1.5 或 2.0 mL 无菌低吸附离心管
2. 八联管及管盖
3. 1000 μL,200 μL,100 μL,10 μL 无菌低吸附带滤芯枪头
4. 75 %酒精
5. 医疗用一次性利器盒
6. 核酸清除剂,联系本公司订购
1. 单人桌面无菌超净工作台(SSD-1)
2. 迷你离心机
3. 漩涡振荡器
4. 荧光定量 PCR 仪
5. 1000 μL,200 μL,100 μL,10 μL 移液枪
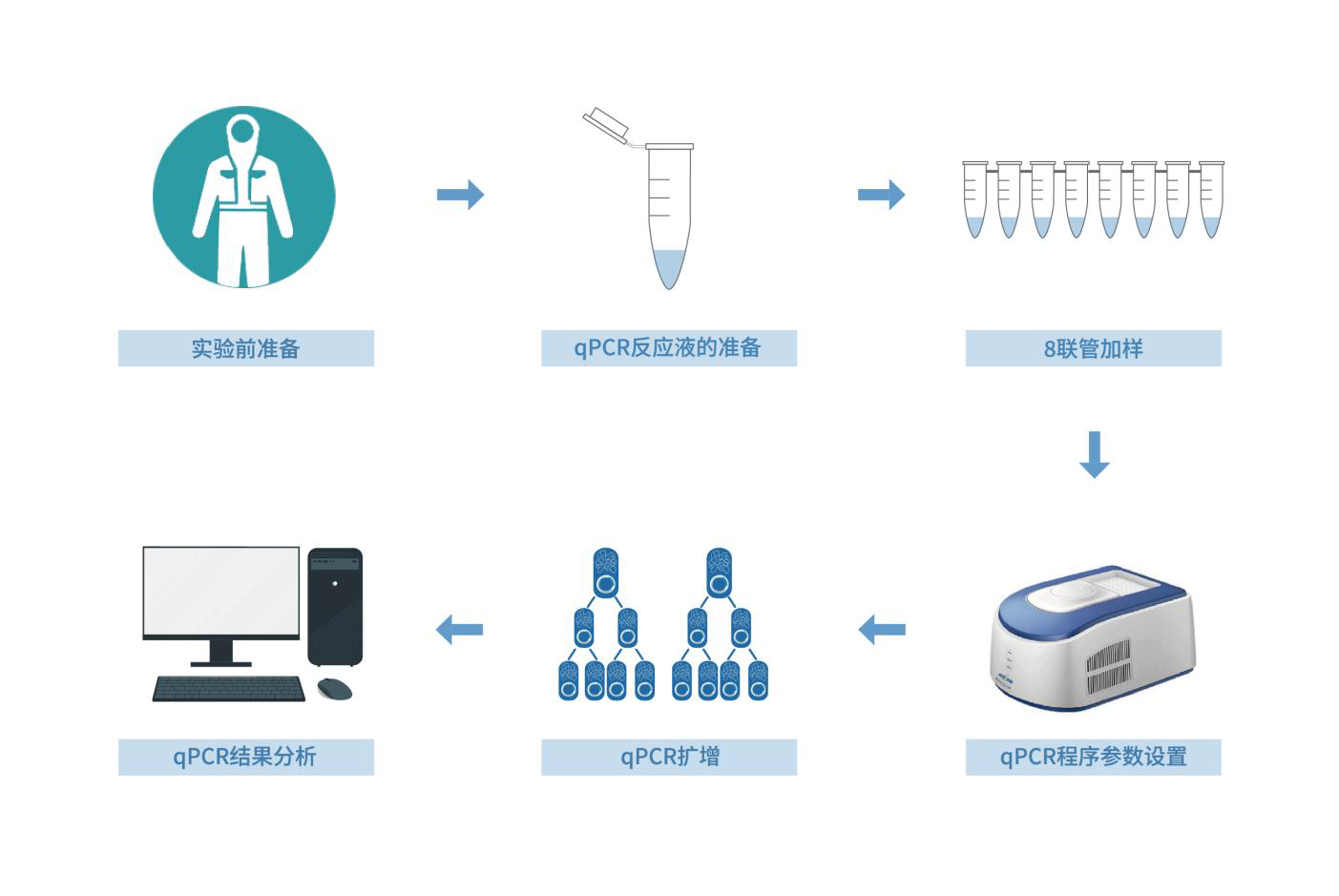
图 1 操作流程示意图
1. 穿戴适当的工作及保护服, 至少穿戴无 DNA 污染的工作服、一次性反穿衣、一次性乳胶手套、一次性无纺布帽子和医用口罩。
2. 工作区及环境采取适当地消毒,去除残留核酸。至少工作台面、移液枪、枪头、八联管及管盖、离心管及离心管架紫外照射时长不少于 1小时,使用核酸清除剂、75%酒精全面擦拭消毒。
3. 将试剂盒从冰箱-18 ℃以下区域转移至 2-8 ℃区域融化,涡旋振荡混匀并瞬时离心。
4. 参考《MicroSHENTEK®真菌&细菌 DNA 提取纯化试剂盒(磁珠法)说明书》要求进行分区:分为阴性区、待测样品区、阳性区。分别在各区域单人桌面无菌超净工作台(SSD-1)中操作。

阴性区:试剂配制区域&NCS、NTC 阴性质控加样区域;待测样品区:待测样品加样区域;
阳性区:PCS、PC 阳性质控加样区域。
1. 根据所要检测样品的数量,计算所需反应孔数,一般做 2 个重复孔。反应孔数=(1 个阳性质控 PC + 1 个无模板对照 NTC + 1 个阴性对照样品 NCS + 1 个阳性对照样品 PCS + N 个待测样品)× 2
2. 根据反应孔数计算所需的 qPCR MIX 总量:qPCR MIX 总量 =(反应孔数+2)× 10 μL(含有 2 孔的损失量)
3. 将各试剂根据表 2 所示准备 qPCR MIX:
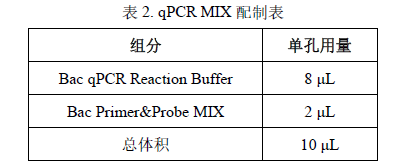
* qPCR MIX 配制应在阴性区无菌超净工作台中操作。
1. 将所有溶液振荡混匀后根据表 3 所示加样,排版方式可参考表 4:
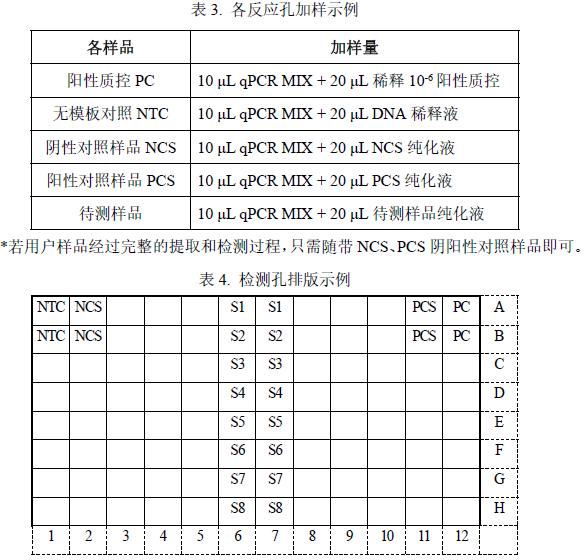
² 该示例表示的是检测 1 个阳性质控 PC、1 个无模板对照NTC、1 个阴性对照样品 NCS、1 个阳性对照样品 PCS、8 个待测样品。每个检测做 2个重复孔。
² 实际检测时可根据样品多少,参照此示例进行排版加样。
*严格注意操作顺序:应当依次在阴性区完成 NTC 和 NCS 加样及封闭,待测样品区完成待测样品加样及封闭,阳性区完成 PCS 加样及封闭,最后完成稀释 10-6 PC 加样及封闭。(注意:阳性质控 PC 需要按 10 倍梯度稀释 106之后加样,为避免实验污染,必须在实验最后一步进行稀释操作)
将八联管用管盖封闭,轻微震荡混匀,短时间快速离心 10 秒后放入 qPCR仪,接着进行 qPCR 程序设置:
l SHENTEK-96S 实时荧光 PCR 检测系统、软件版本 8.2.2 为例。
1. 点击“实验向导”。
2. “孔板编辑”页面中选择步骤 1:选择反应孔。
3. 选择步骤 2:选择项目中的“Micro-Fun&Bac”程序。
4. “实验运行”页面中点击“开始”运行程序。
l 其他荧光定量 qPCR 系统推荐程序设置如下:
1. 创建空白新程序,选择绝对定量检测模板。
2. 创建新检测探针,命名为“细菌检测”,选择报告荧光基团为 FAM。
3. 设置三步法反应程序:
95 ℃ 15 秒,55 ℃ 30 秒,72 ℃ 1 分钟(读取荧光),45 个循环;
反应体积 30 μL。
若真菌&细菌使用同一台荧光定量 qPCR 系统检测,则需按照真菌检测程序增加 25℃ UNG 酶作用 10 分钟和采用FAM 和VIC 双通道检测。
l 以 SHENTEK-96S 实时荧光 PCR 检测系统、软件版本 8.2.2 为例。
1. “孔板编辑”页面中步骤 3:定义反应孔,将 NTC 孔的样品类型设置为无模板对照,PC 孔、PCS 孔设置为阳性对照,NCS 孔设置为阴性对照,待测样品孔设置为待测样品。
2. 在“实验分析”页面点击![]() , 在“反应孔信息表中”可读取无模板对照 NTC、阴性对照样品 NCS、阳性对照样品 PCS、阳性质控 PC、待测样品的检测值。
, 在“反应孔信息表中”可读取无模板对照 NTC、阴性对照样品 NCS、阳性对照样品 PCS、阳性质控 PC、待测样品的检测值。
l 以 Roche LightCycler 480 Ⅱ、软件版本 1.5 为例。
1. 在 Subset Editor 的左下方点击“+”选项,然后选择相对应上样孔,确定后点击右下方的“Apply”选项保存。
2. 在 Sample Editor 的 Sample Name 一栏中命名相对应上样孔的名称NTC、NCS、S、PCS、PC。
3. 在 Analysis 中选择 Abs Quant/Fit Points 分析类型,点击“√”选项进入界面,在 Noise Band 界面下方选择 Noiseband(Fluoresc),通过手动改变 Noise Band 使阴阳性样品区分(此时 Threshold 将与 Noise Band 保持一致),然后点击左下方“Calculate”选项,进行 Ct 值读取。
上述示例结果分析的参数设置仅供参考,具体需依据实验室机型及使用的软件版本进行设定。
1. PC、NTC、NCS、PCS 检测结果应为:

*质控标准应基于实验室验证数据,可从满足检测限要求考虑。
2. 待测样品检测结果判定:
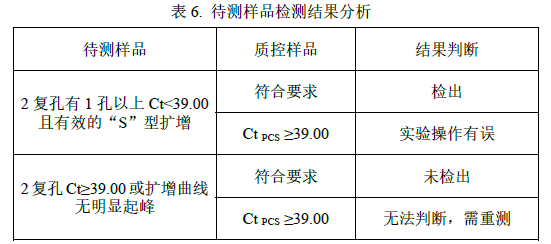
*若阴性质控 Ct 值<39.00>
*阴阳性质控符合要求时,若待测样品 Ct 值<39.00>
*如遇特殊样品或其他异常现象,结果难以判定,可联系湖州申科,咨询具体解决方案。
生效日期:2024 年 02 月 06 日



