

本试剂盒与SHENTEK®病毒核酸提取试剂盒(磁珠法)配套使用,用于检测生物制品中由鼠源细胞(CHO、BHK、NS0 等),动物源性原辅料和实验室环境引入的鼠细小病毒(Minute Virus of Mice,MVM)污染。
该试剂盒检测覆盖4 种鼠细小病毒毒株(i,p,m,c)。检测灵敏度达到50 copies/反应。检测特异性强,与工程细胞(CHO、VERO、293T、MDCK、NS0、Sf9),工程菌(大肠杆菌、毕赤酵母)无交叉扩增。试剂盒内含内部质控IC,配合SHENTEK®病毒核酸提取试剂盒(磁珠法)可高效在细胞、血清等复杂基质样品中回收病毒核酸。
n试剂盒简介
SHENTEK®鼠细小病毒(MVM)核酸检测试剂盒(PCR-荧光探针法)与 SHENTEK®病毒核酸提取试剂盒(磁珠法)配套使用,用于检测生物制品中由鼠源细胞(CHO、BHK、 NS0 等),动物源性原辅料和实验室环境引入的鼠细小病毒(Minute Virus of Mice,MVM)污染。
该试剂盒检测覆盖 4 种鼠细小病毒毒株(i,p,m,c)。检测灵敏度达到 50 copies/反应。检测特异性强,与工程细胞(CHO、VERO、293T、MDCK、NS0、Sf9),工程菌(大肠杆菌、毕赤酵母)无交叉扩增。试剂盒内含内部质控 IC,配合 SHENTEK®病毒核酸提取试剂盒(磁珠法)可高效在细胞、血清等复杂基质样品中回收病毒核酸。
n试剂盒组分
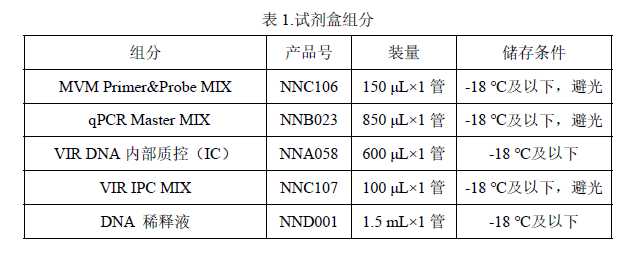
50 Reactions。
规定储存条件下 24 个月,具体详见试剂盒标签。
1. SHENTEK-96S 定量 PCR 系统
2. 7500 Real-Time PCR System
3. Roche LightCycler 480 Ⅱ
1. 1.5 mL 或 2.0 mL 无菌 DNase/RNase-free 低吸附离心管
2. 96 孔 qPCR 板或八联管
3. 1000 μL,200 μL,100 μL,10 μL DNase/RNase-free 低吸附带滤芯枪头
4. 病毒核酸提取试剂盒(货号:1506730)
5. MVM 病毒阳性对照品(货号:1506747),联系本公司订购
1. 生物安全柜
2. 迷你离心机
3. 漩涡振荡器
4. 荧光定量 PCR 仪
5. 1000 μL,200 μL,100 μL,10 μL 移液枪
图 1 操作流程示意图
1. 穿戴适当的工作及保护服,至少穿戴无 DNA 污染的工作服、一次性反穿衣、一次性乳胶手套、一次性无纺布帽子和医用口罩。
2. 病毒提取检测和病毒阳性对照品处理建议在P2 实验室和生物安全柜中进行。
3. 检测过程中严格使用无核酶的试剂和耗材。
4. 需要使用的试剂提前取出置于冰上融解并充分混匀。
(二)样品提取:
使用病毒核酸提取试剂盒对样品中的病毒核酸提取纯化。
取牛血清或 107 及以下细胞样品体积 200 μL,加入样品处理液(1/10 样品体积用量),涡旋震荡混匀,快速离心 3-5 s,室温处理 5 min。450×g 离心30 min(4 ℃),吸取上清转移到新离心管中。下一步进行样品消化。
其他类型样品可直接进行样品消化处理。特殊类型基质样品可咨询湖州申科技术支持!
阳性对照品(PCS)
取 1 管 MVM 阳性对照品作为 PCS,在样品消化步骤同待测样品一起进行相同的样品前处理,制备成 PCS 纯化液用于检测。
阴性对照品(NCS)
取 DNA 稀释液或 1×PBS(同待测样品体积)作为阴性对照 NCS,在提取阶 段和同批待测样品一起进行相同的样品前处理,制备成 NCS 纯化液用于检测。
内部质控(IC)
NCS,PCS 和所有待测样品在提取阶段样品消化时加入 VIR DNA 内部质控(IC) ,提取纯化后进行 qPCR 检测。
NCS,PCS 和所有处理后的待测样品加入 100 μL 蛋白酶 K 缓冲液和 50 μL蛋白酶 K,再加入 10 μL VIR DNA 内部质控(IC),涡旋震荡混匀,快速离心 3-5 s,55 ℃ 孵育 30 min。孵育完成后加入 10 μL 的 5M NaCl 和 10 μL 的助沉剂 Ⅰ 工作液(即配即用),涡旋震荡混匀,快速离心 3-5 s。
建议使用 rHCD purify®前处理系统,按照 SHENTEK®病毒核酸提取试剂盒说明书流程进行病毒核酸提取。
(三)qPCR 反应液准备:
1. 根据所要检测样品数量,计算所需反应孔数,一般做 2 个重复孔/样。反应孔数 =(1 个无模板对照 NTC + 1 个阴性对照样品 NCS+1 个阳性对照样品 PCS+ N 个待测样品)×2
2. MIX 总量计算:根据反应孔数计算本次所需的 qPCR MIX 总量。MIX 总量 =(反应孔数 + 2)× 20μL(含有 2 孔的损失量)
3. 根据表 2 配制表准备各试剂 qPCR MIX 用量。
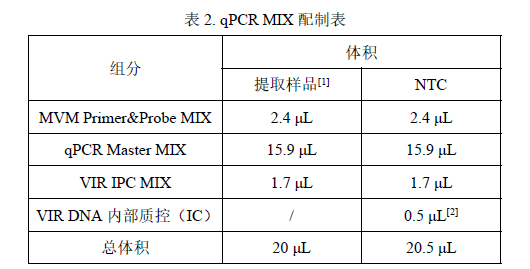
[1]提取样品包括待测样品,NCS 和 PCS,IC 作为内部质控在提取检测阶段加入到样品中。
[2]NTC 作为检测时的阴性对照需要配置单独加内部质控(IC)的 MIX 进行检测。
1. 将所有溶液振荡混匀后按表 3 和表 4 所示加样:
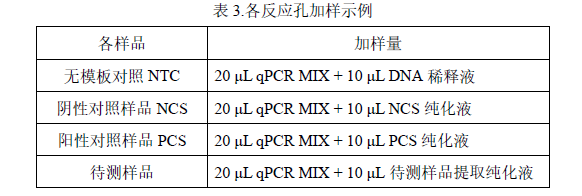
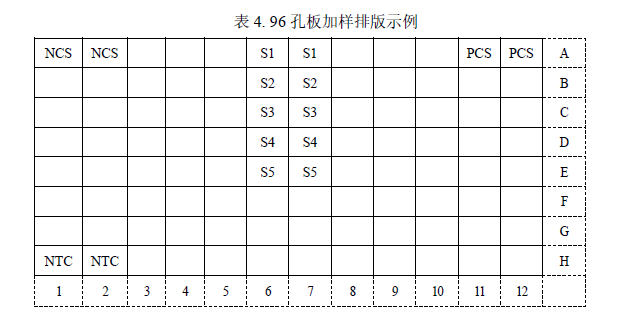
·该示例表示的是检测 1 个阴性对照样品 NCS、1 个无模板对照 NTC、1个阳性对照样品 PCS、5 个待测样品。每个检测做 2 个重复孔
·实际检测时可根据样品多少,参照表 4 示例进行 96 孔板排版加样。
将八联管用配套管盖盖紧或 96 孔板用光学膜封闭,轻微震荡混匀,短时间快速离心 10 秒后放入 qPCR 仪,接着进行 qPCR 程序设置:
1. 点击“实验向导”。
2. “孔板编辑”页面中选择步骤 1:选择反应孔。
3. 选择步骤 2:选择项目中的“MVM 检测”程序。
4. “实验运行”页面中点击“开始”运行程序。
l 其他定量 PCR 系统程序设置如下:
1. 创建空白新程序,选择绝对定量检测模板。
2. 创建新检测探针,命名为“MVM”,选择报告荧光基团为 FAM,猝灭荧光基团为 None;创建 VIC 探针,选择报告荧光基团为 VIC,猝灭荧光基团为 None,检测参比荧光为 ROX(可选)。
3. 设置 qPCR 反应程序:
95 ℃ 15 秒,60 ℃ 1 分钟(读取荧光),40 个循环;
反应体积 30 μL。
1. “孔板编辑”页面中步骤 3:定义反应孔,将 NTC 孔的样品类型设置为无模板对照,NCS 孔设置为阴性对照,PCS 孔、待测样品孔设置为待测样品。
2. 在“实验分析”页面点击![]() , 在“反应孔信息表中”可读取无模板对照 NTC、阴性质控 NCS、阳性质控 PCS、待测样品的检测值。
, 在“反应孔信息表中”可读取无模板对照 NTC、阴性质控 NCS、阳性质控 PCS、待测样品的检测值。
1. 在 Results 的 Amplification Plot 面板中,将 Threshold 设置为 0.02,点击 Analyze,此时可初步查看扩增曲线的形态是否正常。
2. 在 Results 的 Plate 面板中,将无模板对照 NTC 孔的 Task 一栏设置为 NTC,将阴性对照 NCS 孔、待测样品孔、阳性对照 PCS 孔的 Task一栏设置为 Unknown,并且在相应的 Sample Name 一栏中命名为 NTC、NCS、S、PCS,之后点击![]() 。
。
3. 在 Results 的 Report 面板中,Mean Quantity 一栏可读取无模板对照NTC、阴性对照 NCS、待测样品、阳性对照 PCS 的检测值。
上述示例结果分析的参数设置仅供参考,具体需依据实验室机型及使用的软件版本进行设定,一般也可由仪器自动判读。
1. NTC、NCS、PCS 检测结果参考表 5:
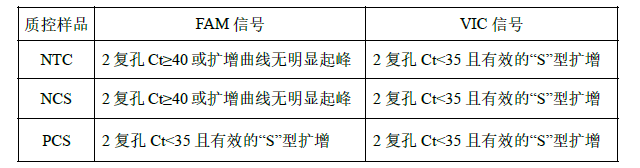
*质控标准应基于仪器和实验室验证数据,可从满足检测限要求考虑。
2. 待测样品检测结果判定参考表 6:
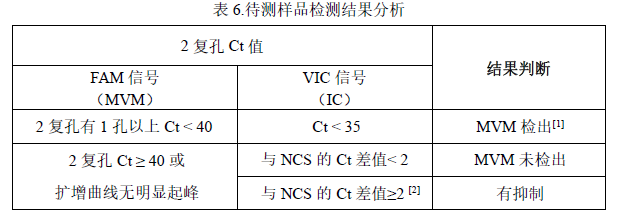
[1]分析 FAM 信号的检测值,2 复孔有 1 孔以上 Ct < 40 且有效的“S”型扩增可判定样品中存在 MVM 病毒核酸。
[2 ]比较样品的VIC 信号检测Ct 值与NCS 的Ct 值的差值,大于 2 说明提取检测受到抑制,需重测或对样品进行合适处理消除抑制因子来确定样品是否无病毒检出。
生效日期:2023 年 09 月 19 日



