

产品信息:
• 检测类型:定量检测
• 产品规格:100测试
• 适用样品类型:对来源于常见的HIV-1型慢病毒载体技术制备的人源细胞产品目的基因拷贝数进行分析。
• 线性范围:CAR/TCR(2.33×101~2.33×107pg/μL;R2≥0.990;扩增效率为94.9%),SCG(2.33×101~2.33×107copies/μL;R2≥0.990;扩增效率为94.8%)
• 样品回收率:50-150%
• LLOQ:CAR\TCR(2.33×101 copies/μL),SCG(5.825×101 copies/μL)
• 专属性:不受CHO、Vero、NS0和MDCK等常见工程细胞基因组DNA的干扰。
• 精密度:中间精密度及重复性实验CV值均在15%以内。
• 耐用性:至少反复冻融5次检测性能不受影响。
• 仪器适用性(包括但不限于以下设备):湖州申科SHENTEK-96S、Thermo ABI7500、Bio-Rad CFX-96、博日FQD-96A
产品特点:
• 操作简单:搭配SHENTEK前处理设备及试剂盒,可实现自动化提取及检测。
• 灵敏度高:定量限CAR\TCR(2.33×101 copies/μL),SCG(5.825×101 copies/μL),满足实际检测需求。
• 性能稳定:试剂盒重复实验间结果稳定,均满足精密度需求。
• 质量可控:试剂盒按照药典、法规完成各项检测指标的性能验证。
质量保证:
• 建立ISO13485质量管理体系,具有完善的从研发、生产、质检的产品开发流程。
• 生产高度设备化,历史多批次生产稳定,供应链完善。
SHENTEK® CAR/TCR 基因拷贝数检测试剂盒适用于定量检测来源于常见的 HIV-1型慢病毒载体技术制备的人源细胞产品中目的基因的拷贝数,如 CAR-T 和 TCR-T 细胞基因组中 CAR 或 TCR 基因的拷贝数。
本试剂盒基于荧光探针法,采用多重 qPCR 的方法分别检测转移质粒上与整合或表达功能相关的 DNA 序列和人体细胞中单拷贝基因(Single Copy Gene,SCG)的方法,计算得到样品中平均每个细胞的目的基因拷贝数,如 CAR 或 TCR 基因拷贝数水平。本试剂盒检测快速,专一性强,性能可靠,针对慢病毒载体技术具有通用性。试剂盒配套有本公司构建的定量参考品。
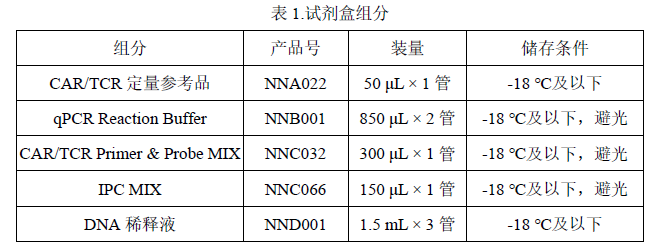
100 Reactions。
规定储存条件下 24 个月,具体详见试剂盒标签。
Ø SHENTEK-96S 实时荧光 PCR 检测系统
Ø 7500 Real-Time PCR System
Ø CFX96 定量 PCR 系统
Ø Linegene 9600plus 定量 PCR 系统
Ø 1.5 mL 低吸附无菌离心管
Ø qPCR 反应板或条
Ø 1000 μL,100 μL,10 μL 无菌有滤芯低吸附枪头
Ø 荧光定量 PCR 仪
Ø 1000 μL,100 μL,10 μL 移液枪
CAR/TCR 定量参考品浓度标注于管壁标签,请确认后再进行稀释。通过以下公式来换算拷贝数:
质粒拷贝数(copies/μL)=6.02 × 1014 × 质粒浓度(ng/μL)/(质粒碱基数 × 660)得到:CAR/TCR 和 SCG 基因拷贝数均为 2.33 × 108 copies /μL
用试剂盒中提供的 DNA 稀释液将 CAR/TCR 定量参考品进行 10 倍梯度稀释,具体操作如下:
1. 将试剂盒中的定量参考品和 DNA 稀释液置于冰上或 2-8 ℃条件下融化,待完全融化后,轻弹数下混匀,短时间快速离心 3-5 s,如此重复 3 次。
2. 取 6 支干净的 1.5 mL 离心管,分别标记为 ST0,ST1,ST2,ST3,ST4,ST5。
3. 在 ST0 管中用 DNA 稀释液将定量参考品稀释 10 倍,得到 ST0,振荡混匀后短时间快速离心 3-5 s,重复 3 次以确保定量参考品与 DNA 稀释液充分混匀。
4. 在 ST1,ST2,ST3,ST4,ST5 管中分别加入 90 μL DNA 稀释液。
5. 按表 2 依次进行 5 次稀释操作。
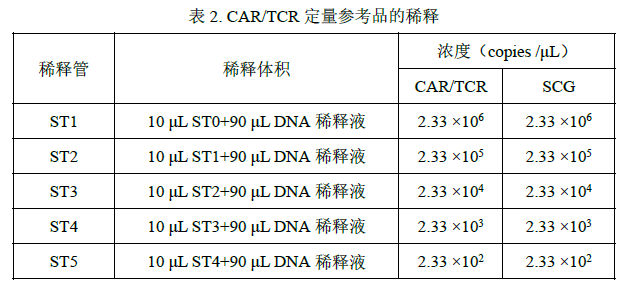
已融化未使用的 DNA 稀释液可保存于 2-8 ℃。
若 DNA 稀释液中有析出,建议于 37 ℃条件下进行孵育。
1. 建议随行阴性质控样品 NCS(DNA 稀释液)同样品一起进行前处理,制备成阴性质控 NCS 纯化液。
2. 根据所要检测的标准曲线及待测样品数量,计算所需反应孔数,一般做 3 个重复孔/样。反应孔数=(5 个浓度梯度的标准曲线+1 个无模板对照NTC+1 个阴性质控样品NCS+待测样品数)× 3
3. 根据反应孔数计算本次所需的 qPCR MIX 总量(含有 2 孔的损失量):
4. 各试剂置于冰上或 2-8 ℃条件下融化,轻微振荡混匀,按表 3 所示加样:
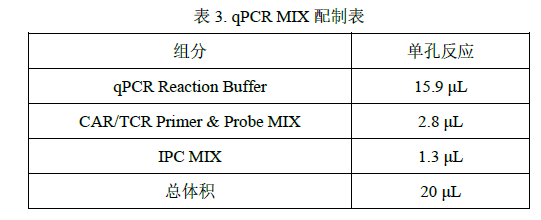
1. 上述各试剂置于冰上,轻微震荡混匀,按表 4 所示加样:

加样完成后每孔总体积为 30 μL。
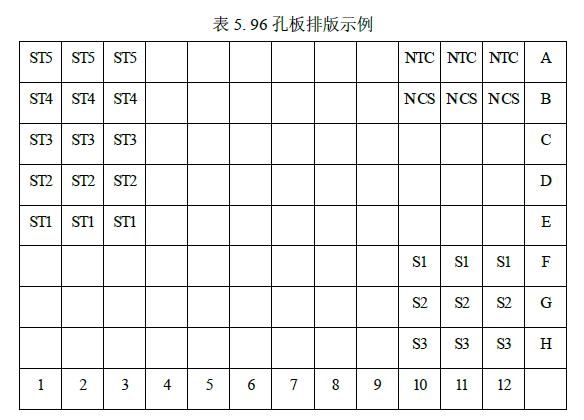
该示例表示的是检测 5 个浓度梯度的标准曲线(ST1-ST5)、1 个无模板对照 NTC、 1 个阴性质控样品 NCS、3 个待测样品(S1-S3)。每个检测做 3 个重复孔。
实际检测时可根据样品多少,参照此示例进行 96 孔板排版加样。待测样品的每孔上样总量推荐 5 ng-30 ng 区间,可根据预实验情况适当调整。
2. 将 96 孔板用光学膜封闭,轻微震荡混匀,短时间快速离心 10 s 后放入 qPCR 仪。
² SHENTEK-96S 实时荧光 PCR 检测系统、软件版本 8.2.2 为例。
1. 点击“实验向导”。
2. “孔板编辑”页面中选择步骤 1:选择反应孔。
3. 选择步骤 2:选择项目中的“CAR-TCR 拷贝数检测”程序。
4. “实验运行”页面中点击“开始”运行程序。
² 其他定量 PCR 系统程序设置如下:
1. 创建空白新程序,选择绝对定量检测模板。
2. 创建新检测探针,命名为 CAR 或 TCR,选择报告荧光基团为 FAM,猝灭荧光基团为 none;创建新检测探针,命名为 SCG,选择报告荧光基团为 CY5,猝灭荧光基团为 none;创建新检测探针,命名为 IPC,选择报告荧光基团为 VIC,猝灭荧光基团为 none;检测参比荧光为 ROX(可选)。
3. 设置两步法反应程序:95 ℃预变性 10 min;95 ℃ 15 s,60 ℃ 1 min(读取荧光),40 个循环;反应体积 30 μL。
² 以 SHENTEK-96S 实时荧光 PCR 检测系统、软件版本 8.2.2 为例。
1. “孔板编辑”页面中步骤 3:定义反应孔,将标准曲线孔的选择样品类型设置为标准品,并在标品赋值中分别根据表 2 赋值,“通道 1”分别设为 2.33 ×106、2.33 ×105、 2.33 ×104、2.33 ×103,2.33 ×102,“通道 4”分别设为 2.33 ×106、2.33 ×105、2.33 ×104、2.33 ×103,2.33 ×102(单位为 copies/μL),并且在相应的“样本名称”中命名为 ST1、ST2、 ST3、ST4、ST5。
2. 待测样品将样品类型设置为待测样品,NTC 将样品类型设置为无模板对照。
3. 在“实验分析”页面点击![]() ,可读取标准曲线的斜率、截距、相关系数、扩增效率。
,可读取标准曲线的斜率、截距、相关系数、扩增效率。
4. 在“反应孔信息表中”可读取无模板对照 NTC、阴性质控 NCS、待测样品的检测值,单位为 copies/μL。
² 以 7500 Real-Time PCR System、软件版本 1.4 为例。
通过选择不同的探针,对 CAR 或 TCR 基因及 SCG 基因进行分析。
1. 在 Results 的 Amplification Plot 面板中,将 Threshold 设置为 0.02,点击 Analyze,此时可初步查看扩增曲线的形态是否正常。
2. 在 Results 的 Plate 面板中,将标准曲线孔的 Task 一栏设置为 Standard,并且在 Quantity 一栏分别根据表 2 赋值,例如 SCG 设为 2.33e+006、2.33e+005、2.33e+004、 2.33e+003、2.33e+002(单位为 copies/μL),并且在相应的 Sample Name 一栏中命名为 ST1、 ST2、ST3、ST4、ST5。
3. 在 Results 的 Plate 面板中,将无模板对照 NTC 孔的 Task 一栏设置为 NTC,将待测样品孔的 Task 一栏设置为 Unknown,并且在相应的 Sample Name 一栏中命名为 NTC、 NCS、S 之后点击。
4. 在 Results 的 Standard Curve 面板中,可读取标准曲线的斜率( Slope)、截距(Intercept)、R2。
5. 在 Results 的 Report 面板中,Mean Quantity 一栏可读取无模板对照 NTC、阴性质控 NCS、待测样品的 CAR 或 TCR 和 SCG 检测值,单位为 copies/μL。
6. 无模板对照 NTC 检测结果应大于标准曲线最低浓度点的 Ct 值。
7. 分析 IPC 的 Ct 值,正常情况下样品的 Ct-IPC 值应该与阴性质控 NCS 的 Ct-IPC值一致或±1。如样品的 Ct-IPC 值与阴性质控 NCS 的 Ct-IPC 值相比明显增大,则表明样品可能存在抑制。
8. 结果计算:CAR 或 TCR copies/cell = 2 × CAR 或 TCR/SCG
上述示例结果分析的参数设置仅供参考,具体需依据实验室机型及使用的软件版本进行设定,一般也可由仪器自动判读。
修订日期:2023 年 03 月 23 日
生效日期:2023 年 03 月 29 日



